جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
((بسم رب المهدی عجل الله تعالی فرجه الشریف))
.
گردآورنده اولیه: احمد احمدی
بازنگری ، اصلاح ، ویرایش و به روز رسانی : ناصر فخار نوغانی
آخرین به روز رسانی جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه : اسفندماه ۱۳۹۸
.
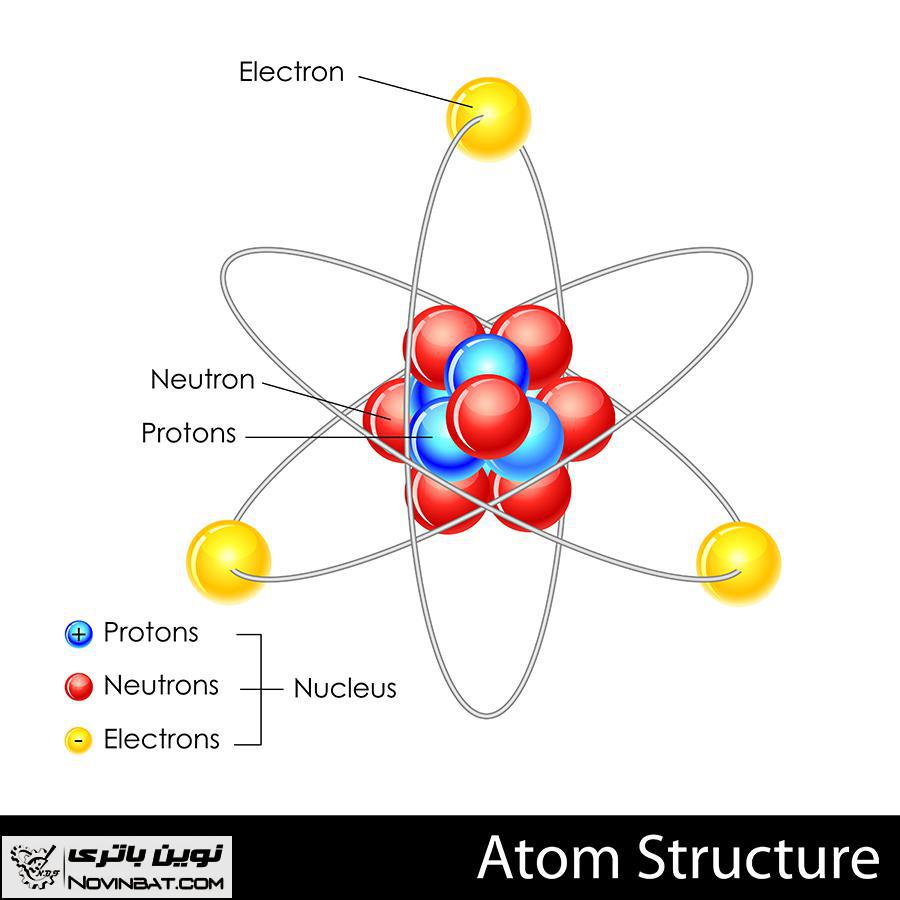
الکتریسیته، نوترون و پروتون
همه اجسام (مواد مرکب) در طبیعت از مواد مختلفی ساخته شده اند. این مواد مرکب نیز خود از چندین ماده مختلف و هر یک از این مواد مختلف نیز از عناصر مختلف دیگری تشکیل شده اند.
بعنوان مثال یک ماده مختلف مانند فلز مفرغ (برنز) از دو عنصر مس و قلع تشکیل شده است که این دو عنصر مس و قلع از این ساده تر نمی شوند و فقط می توان آن را به مولکول های مس و قلع تقسیم نمود بنابر این می توان گفت که عناصر شکل ساده شده همه مواد هستند که قابل تقسیم شدن نیستند و فقط می توان آنها را به مولکول های کوچک تر همان عنصر تقسیم کرد.
پس عناصر خود نیز از قطعات کوچک تری بنام مولکول ساخته شده اند که توسط چشم غیر مسلح قابل دیدن نیستند و اگر بخواهیم مولکول را نیز به قطعات ریزتری تقسیم کنیم به اتم می رسیم که جزء ریزتر مولکول می باشد. اتم ها در این مبحث بیشتر مورد بررسی هستند چرا که دارای اجزای ریزتری بنام الکترون، پروتون و نوترون می باشند.
الکترون نسبت به دو جزء دیگر بیشتر مورد توجه می باشد زیرا که بر اثر حرکات و جا به جایی آن، جریان الکتریسیته برقرار می گردد، به همین دلیل به این جریان، جریان الکتریسیته گفته می شود چرا که از حرکت الکترون ها نشأت گرفته شده است و لازم است قبل از شروع مبحث الکتریسیته نگاهی اجمالی به این سه جزء اتم بیندازیم.
نوترون
مرکزی ترین و سنگین ترین جزء اتم است که به عنوان مرکز ثقل اتم عمل می کند و در جریان الکتریسیته اهمیت چندانی ندارد و دارای بار الکتریکی خنثی می باشد.
پروتون
مانند گوشتی اطراف نوترون را فرا گرفته است و با نوترون هسته را تشکیل می دهد. از نوترون سبک تر است و بدلیل اینکه دارای بار الکتریکی مثبت می باشد باعث نگه داشتن الکترون ها در اطراف هسته می شود. مقدار نیروی جاذبه مثبت پروتون، باعث رسانا شدن و نارسانا شدن عنصر می گردد.
الکترون
سبک ترین جزء اتم می باشد که در لایه های خاصی (اوربیتال) به دور هسته اتم می گردد و دارای بار منفی می باشد.
الکترون توسط نیروی مثبت هسته که توسط پروتون بر آن اعمال می شود در اطراف هسته باقی می ماند و به دلیل چرخشی که به دور خود انجام می دهد مانع جذب آن توسط پروتون ها می شود.
در عین حال که دارای کمترین وزن می باشد ولی از نظر حجم دارای حجمی تقریباً ۱۸۷۳ برابر پروتون می باشد و بیشتر مسائل موجود الکتریسیته بر اساس رفتار الکترون توجیه می شود.
اگر بخواهیم اتم را به چیزی تشبیه کنیم می توانیم از منظومه شمسی نام ببریم که در آن خورشید نماد هسته اتم می باشد و سیاره هایی که دور آن می چرخند همانند الکترون ها می باشند که همزمان که به دور خورشید می چرخند به دور خود نیز گردش دارند.
.
مواد هادی و نیمه رسانا و عایق
دورترین لایه نسبت به هسته را لایه والانس یا لایه ظرفیت می نامند که تعداد الکترون های موجود در آن لایه، مواد هادی و نیمه هادی و عایق را مشخص می نماید.
۱- مواد هادی: اگر تعداد الکترون ها در لایه والانس ۱ تا ۳ الکترون باشد ماده موجود رسانا می باشد.
۲- مواد نیمه رسانا: اگر تعداد الکترون ها در لایه والانس ۴ الکترون باشد ماده موجود نیمه رسانا می باشد.
۳- مواد عایق: اگر تعداد الکترون ها در لایه والانس ۵ تا ۸ الکترون باشد ماده موجود عایق می باشد.
نکته: در طبیعت مواد ۱۰۰% عایق یا رسانا وجود ندارد.
مدار الکتریکی
اگر ما در جایی تجمع الکترون و در جایی دیگر نبود الکترون داشته باشیم (که از آن تحت عنوان حفره نام برده می شود) و از ماده رسانایی که باعث ارتباط بین الکترون ها و حفره ها شود، استفاده نماییم، الکترون ها از محل تجمع الکترون ها به سمتی که فاقد الکترون است (حفره) حرکت می کنند که همین عمل سبب جریان یافتن الکترون ها می شوند.
برای درک بهتر این مطلب به مثال باتری توجه نمایید:
یک باتری را در نظر بگیرید.
یک سمت این باتری قطب مثبت و سمت دیگر قطب منفی می باشد.
در قسمتی که پلاریته (قطب) مثبت قرار دارد، دارای حفره هستیم و قسمتی که پلاریته منفی قرار دارد، شاهد تجمع الکترون ها هستیم.
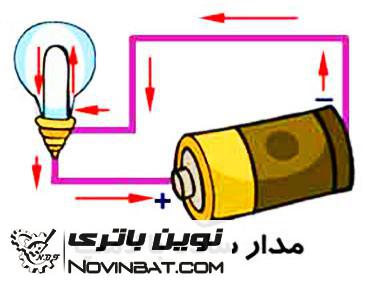
وقتی ما لامپی را به این دو پلاریته متصل می کنیم، الکترون ها به دلیل رسانا بودن لامپ، از سمت تجمع الکترون ها حرکت می کنند تا به سمتی که حفره وجود دارد برسند و چون در بین راه از لامپ عبور می کنند باعث روشن شدن آن می شوند و به سمت حفره ها می رسند.
وقتی که همه الکترون ها به سمت حفره ها حرکت کردند در این حالت چون دیگر الکترونی برای حرکت کردن نمانده است، لامپ (مصرف کننده) خاموش شده و باتری به اصطلاح تمام شده است (باتری دشارژ شده است).
این ارتباط بین الکترون ها و حفره های موجود در یک منبع که باعث کار کردن مصرف کننده می شوند را مدار الکتریکی می گویند. شکل زیر تصویر ساده یک منبع الکتریکی را نشان می دهد:
نکته: در حالت علمی و تئوری حرکت الکترون ها از منفی به مثبت می باشد ولی به صورت قراردادی برای توجیه بسیاری از مسائل الکترونیک، حرکت حفره ها را از مثبت به منفی می گیرند.
بیشتر مشکلاتی که ممکن است برای یک مدار الکتریکی اتفاق بیفتد عبارت است از:
۱- قطعی مدار
۲- برق دزدی در مدار
۳- اتصال کوتاه شدن مدار
موارد فوق عملکرد مدار الکتریکی را مختل می کند و ممکن است شاهد رخدادهای دیگری مثل سوختن سیم کشی یا روشن نشدن مصرف کننده یا دشارژ شدن منبع تغذیه باشیم که تشخیص عیب و مشکل مدار الکتریکی، ممکن است مشکل و یا وقت گیر باشد.
پس از شناخت مدار الکتریکی لازم است که با سه کمیت بسیار مهم که در مدارهای الکتریکی بسیار تاثیر گذار هستند آشنا شویم که عبارتند از:
۱- اختلاف پتانسیل: به حرکت الکترون ها از جایی که تعداد آنها بسیار زیاد است (قطب منفی) به جایی که تعدادشان کمتر است (قطب مثبت) اختلاف پتانسیل الکتریکی می گویند. جریان الکتریکی همواره از سمتی که پتانسیل الکتریکی بیشتری دارد به سمتی که پتانسیل الکتریکی کمتری دارد برقرار می شود.
۲- شدت جریان: شدت جریان الکتریکی، مقدار بار الکتریکی خالصی است که در واحد زمان از سطح مقطع خاصی از رسانا عبور می کند.
شدت جریان معمولاً در فرمول ها با نماد I نمایش داده می شود.
۳- مقاوت الکتریکی: مقاوت یک عنصر الکتریکی دو پایه است که مطابق قانون اهم هنگامی که جریان الکتریکی از آن عبور کند بین پایه هایش اختلاف ولتاژ ایجاد می شود.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
باتری خودرو
باتری ها مولد هایی هستند که انرژی شیمیایی را تبدیل به انرژی الکتریکی می کنند.
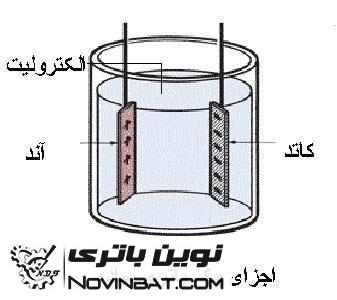
باتری ها معمولاً از کنار هم قرار دادن حداقل دو صفحه فلزی (یا آلیاژی) متفاوت در داخل یک محلول شیمیایی بوجود می آیند.
یکی از این دو صفحه دارای خاصیت الکترون دهی بیشتر (آند) و دیگری دارای خاصلیت الکترون گیری بیشتر (کاتد) می باشد. به عبارت دیگر در یک سِل الکتروشیمیایی آند، الکترودی است که در آن اکسیداسیون رخ میدهد یا به عبارت دیگر در آن الکترون آزاد میشود.
با همین تعریف، کاتد، الکترودی است که در کنار آن واکنش احیا صورت میگیرد یا به عبارت دیگر الکترون مصرف میشود. محلول شیمیایی که باعث ایجاد ارتباط بین این دو صفحه می گردد، الکترولیت نامیده می شود.
نکته: از آنجا که در باتریها جای آند و کاتد حین فرآیند شارژ و دشارژ تغییر میکند، سازندگان باتری کمتر از اصطلاح آند و کاتد استفاده میکنند.
زیرا حین استفاده از این اصطلاحها، همواره لازم است جهت شارژ و دشارژ هم ذکر شود. اما از آنجا که قطب مثبت و منفی همواره ثابت است و تغییر نمیکند، این دو اصطلاح در ادبیات سازندگان باتری، از محبوبیت بیشتری برخوردار شدهاند. به همین دلیل سازندگان باتری، قطبهای باتری را با علامتهای مثبت و منفی نمایش میدهند.
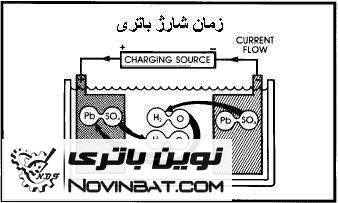
یعنی روی بدنهی باتری علامت مثبت و منفی را حک میکنند اما علامتی برای نمایش آند و کاتد وجود ندارد زیرا قطب مثبت و منفی در یک باتری همواره قطب مثبت و منفی باقی میماند اما کاتد و آند اینگونه نیست. شکل زیر نمایانگر یک باتری ساده در حالت شارژ می باشد:
دسته بندی باتری ها
باتری ها را به روش های مختلفی دسته بندی می کنند. در ادامه مهم ترین روش های دسته بندی آمده است.
از نظر حالت الکترولیت

۱- الکترولیت این نوع باتری ها جامد می باشد مانند باتری های قلمی (Dry-باتری خشک).
۲- دارای الکترولیت مایع می باشند مثل باتری مورد استفاده در خودروها (Wet-باتری تر). نوع جدید این دسته از باتری ها با نام باتری سیلد یا بدون نیاز به نگهداری (Maintenance Free یاLow Maintenance Free ) تولید می گردد.
توجه: نوع دیگری از باتری های به بازار ارائه شده وجود دارد که الکترولیت آن نه کاملاً جامد مانند باتری قلمی است و نه کاملاً مایع مانند باتری های خودرویی، درحالی که الکترولیت این نوع باتری ها مانند ژل می باشد.
نمونه این دسته از باتری ها، باتری های ساکن (UPS) یا باتری های مخابراتی یا باتری های پنل های خورشیدی (Solar) هستند که شاید بتوان این دسته از باتری ها را در دسته باتری های خشک قرار داد.
از نظر جنس الکترولیت و صفحات
معمولاً باتری های مخصوص خودرو از نوع باتری های سربی-اسیدی می باشند و دلیل آن این است که اولاً هزینه ساخت آن کمتر از نوع مشابه آن است و دوماً محدوده دمای مناسب برای بهترین کارایی آن، نسبت به سایر باتری ها گسترده تر است و سوماً آمپر و ولتاژ آن نیز در آن محدوده دمایی مناسب، بالاتر از نمونه های مشابه می باشد.
از این پس منظور ما از عبارت باتری، همان باتری سربی-اسیدی می باشد.
جدول زیر میزان تولید ولتاژ انواع باتری ها، در هر خانه باتری را نشان می دهد:
| نوع باتری | سربی-اسیدی | نیکل-کادمیوم | نیکل-آهن | سدیم-گوگرد |
| ولتاژ هر خانه باتری | ۲ ولت | ۱٫۲ ولت | ۱٫۲ ولت | ۲ ولت |
همانطور که ملاحظه کردید باتری های سربی-اسیدی و باتری های سدیم-گوگرد بیشترین میزان تولید ولتاژ در هر خانه باتری را دارا می باشند اما تولید باتری های سربی-اسیدی به مراتب ارزان تر از باتری های سدیم-گوگرد می باشد (سرب نسبت به سایر فلزات ارزان تر است) بنابراین نوع باتری سربی-اسیدی در خودرو ها متداول می باشد.
چرا خودروها به باتری نیازمند هستند؟
۱- تامین برق مورد نیاز خودرو در زمانی که موتور خاموش است.
۲- تامین برق لازم جهت استارت خودرو
۳- کمک به سیستم شارژ (دینام) در زمانی که تعداد مصرف کننده های الکتریکی بالا می رود (آمپر مصرفی زیاد می شود)
باتری های سربی-اسیدی
همانطور که گفته شد متداول ترین نوع باتری مخصوص خودرو، باتری سربی-اسیدی می باشد.
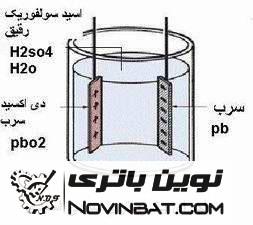
صفحه مثبت از جنس دی اکسید سرب (به آن پراکسید سرب (PbO2) می گویند) و صفحه منفی از جنس سرب (Pb) می باشد. الکترولیت باتری از جنس اسید سولفوریک (H2SO4) رقیق شده با آب (H2O) می باشد.
عملکرد باتری های سربی-اسیدی
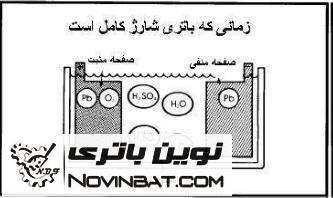
تصاویر زیر به طور خلاصه عملکرد باتری را در زمان های مختلف نشان می دهد:
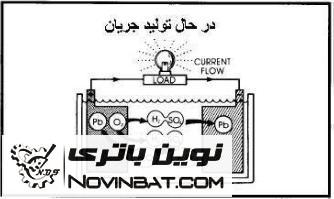
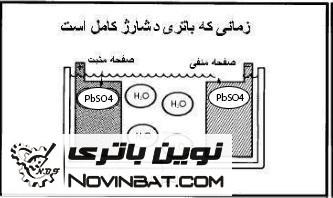
عملکرد فوق نشان می دهد که با شارژ کردن باتری، باتری به همان حالت اولیه خود باز می گردد.
شبکه باتری
شبکه های باتری، قاب های نگهدارنده مواد فعال صفحات باتری هستند.
شبکه های باتری همچنین وضعیت هدایت و انتقال جریان را به صفحات مواد فعال برعهده دارند و علاوه بر این، هدایت و انتقال جریان را از صفحات انجام می دهند. شبکه های باتری از آلیاژ های سرب ساخته شده اند که در آلیاژ های مذبور مقدار اندکی از آنتیموان برای استحکام بخشیدن و سخت کردن سرب نرم استفاده می شود.
امروزه روند کلی در کاهش استفاده از آنتیموان در تولید شبکه های باتری های استارتر قرار گرفته است، زیرا به اعتقاد تولید کنندگان باتری، کاهش استفاده از آنتیموان، میزان تولید گاز (بر اثر واکنش های شیمیایی درون باتری) را کاهش می دهند.
استفاده از سایر فلزات همچون کلسیوم (Ca) یا استرانسیوم (Sr) بجای آنتیموان به منظور ایجاد استحکام و سخت کردن شبکه های باتری سبب می شود که میزان تولید گاز در درون باتری کاهش یابد و آب (الکترولیت باتری) کمتری نیز مصرف شود و همچنین میزان دشارژ خود به خودی باتری نیز کاهش یابد.
مقادیر کمی از سایر فلزات نیز برای بدست آوردن اثرات و نتایج مطلوب گوناگون به آلیاژ اضافه می شوند.
صفحات مثبت و منفی
نخستین گام در تولید صفحات مثبت و منفی، خمیر مالی و قرار دادن مواد بر روی شبکه است.
شبکه باتری دارای ثبات، استحکام و چسبندگی است تا محل مناسبی برای قرار گرفتن ماده خمیری شکل (سرب باتری) مربوط به صفحات باتری باشد. این خمیر مخلوطی از اکسید سرب، اسید سولفوریک، آب و نیز سایر مواد افزودنی مثل الیاف و فیبرهای افزودنی تشکیل شده است که به چسباندن و بهم پیوستن مواد فعال به هم دیگر کمک می کنند.
تفاوت اصلی بین خمیری که برای صفحات مثبت و منفی مورد استفاده قرار می گیرد این است که منبسط کننده ها به خمیر مربوط به صفحات منفی اضافه می شود.
این منبسط کننده ها از آن جهت مورد نیاز هستند که از منقبض شدن مواد ویژه صفحات منفی هنگام استفاده از باتری و همچنین تبدیل آنها به وضعیت غیر فعال متراکم، جلوگیری می کند.
پس از خمیر مالی و خشک کردن صفحات (وضعیتی که به آن هیدروست Hydro Set می گویند) صفحه مثبت به رنگ قهوه ای روشن درمی آید و صفحات منفی به علت وجود مواد منبسط کننده در آنها (به عبارتی بدلیل مخلوط شدن با مواد منبسط کننده) به رنگ خاکستری روشن در می آید.
گام بعدی در جهت تولید صفحات این است که هنگامی که صفحات را در محلول الکترولیت اسید سولفوریک رقیق شده قرار می دهیم، به آنها شارژ اولیه دهیم که از نظر الکتروشیمیایی چنین شارژی اکسید سرب (PbO) مربوط به صفحه مثبت را به دی اکسید سرب (PbO2) تبدیل می کند.
این ماده بسیار مُتخَلِل و پر منفذ است و به همین دلیل الکترولیت آزادانه و به راحتی می تواند به صفحه نفوذ کند.
در این مرحله صفحه مثبت به رنگ قهوه ای تیره (شکلاتی) درآمده است. همان شارژ اولیه ای که در سطور فوق به آن اشاره شد، اکسید سرب مربوط به صفحه منفی را به سرب اسنفجی خاکستری رنگ تبدیل می نماید.
سرب اسنفجی باعث می شود الکترولیت آزادانه و به راحتی نفوذ و رسوخ نماید و این امر سبب می شود که مواد موجود در بخش زیرین و تحتانی همجوار با سطح صفحه در واکنش های شیمیایی شرکت نماید.
اینکه صفحات منفی به رنگ خاکستری تیره در آمده اند. اینکه یک صفحه به صفحه مثبت یا منفی تبدیل شود به جهت امتداد شارژ اولیه بستگی دارد. اگر بر حسب تصادف صفحه ای در معرض جهت معکوس شارژ قرار گیرد، پلاریته (تمایل قطبی) صفحات مذبور که تحت فشار اولیه قرار گرفته اند به نحو معکوس خواهد بود.
صفحاتی که دارای مواد منبسط کننده هستند، به صفحات مثبت دی اکسید سربی مبدل می شوند. چنانچه صفحات منفی سرب اسفنجی حاوی مواد منبسط کننده نباشند، به کارکرد باتری لطمه بزرگی وارد می شود.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
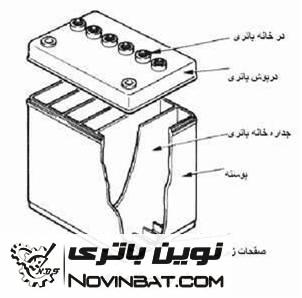
قاب و درپوش باتری (Battery Case and Cover)
جعبه ای که تمام اجزای یک باتری را در خود جای می دهد، قاب باتری نامیده می شود.
قاب یا بدنه (پوسته) باتری ها باید در مقابل اثرات اسید مقاوم باشند. علاوه بر آن باید بتواند تغییرات دما (۵۰- الی ۱۵۰ درجه سانتی گراد) و فشار ناشی از ضربه را تحمل نماید. در گذشته پوسته باتری را از نوعی لاستیک تهیه می کردند اما امروزه معمولاً از پلاستیک های مخصوصی جهت تولید آن استفاده می گردد.
بدنه باتری ها توسط جداره های عمودی معمولاً به شِش خانه تقسیم می شوند.
این قسمت محل قرار گرفتن صفحات مثبت، منفی، عایق، شانه باتری و الکترولیت می باشد. به هر یک از این قسمت ها، یک خانه باتری گفته می شود.
همانطور که ملاحظه می گردد علاوه بر این جداره ها، تعدادی شیار نیز در کف پوسته باتری وجود دارد که دو وظیفه بر عهده دارند. یکی اینکه تکیه گاهی برای صفحات باتری هستند و دیگری اینکه چون پس از مدتی صفحات باتری در اثر فعل و انفعالات شیمیایی ریزش می کنند فاصله بین این شیار ها فضای مناسب جهت ته نشین شدن این رسوبات فراهم می کنند.
جنس درپوش باتری نیز مانند بدنه باتری از نوعی پلاستیک تهیه می شود. بر روی درپوش، محلی برای خروج دو قطب باتری و همچنین نصب درب خانه های باتری تعبیه می گردد.
البته لازم به ذکر است که گاهی درب خانه های باتری از روی درپوش حذف می شوند (برای باتری های بدون نیاز به نگهداری یا سیلد). معمولاً باتری های از نوع ژل (Gel-Cell) که الکترولیت آنها مایع نیستند، احتیاجی به درب خانه باتری ندارند.
تصویر سمت راست نمایانگر باتری اسیدشارژ است که دارای ۶ درب جهت بازدید و کنترل الکترولیت باتری است و تصویر سمت چپ نمایانگر باتری ژل است که فاقد درب جهت بازدید و کنترل می باشد زیرا این دسته از باتری ها نیازمند بازدید و کنترل نمی باشند:

درب خانه باتری (Car Battery Vent Cap)
همانطور که قبلاً ذکر شد معمولاً برای هر خانه باتری یک منفذ در نظر می گیرند که از طریق آن مقدار الکترولیت داخل هر خانه کنترل شود. هر یک از این سوراخ توسط یک در پوش بسته می شوند، که به آن درب خانه باتری می گویند. هر درب خانه باتری باید دارای دو مشخصه مهم باشد که عبارتند از:
۱- اجازه خروج گازهای تولید شده در هر خانه
هنگامی که باتری در حال شارژ شدن توسط دینام (آلترناتور) است بین صفحات مثبت، منفی و الکترولیت، فعل و انفعالات شیمیایی رخ می دهد که این فعل و انفعالات باعث بالا رفتن دما در الکترولیت می گردد (واکنش گرمازا). این افزایش دما باعث افزایش سرعت تبخیر آب موجود در الکترولیت می گردد.
برای خروج بخارهای آب تولید شده در هر خانه باتری لازم است که درب خانه باتری دارای حداقل یک سوراخ یا مجاری خروجی به هوای آزاد باشد که بخار آب تولید شده بتواند از خانه باتری خارج شود. اگر این بخار از خانه خارج نشود فشار در خانه باتری بالا می رود و باعث ایجاد دِفُرمگی (تغییر شکل ظاهری) باتری و حتی انفجار آن می گردد.
بالا رفتن فشار در خانه باتری باعث ایجاد سوراخ های ریزی در ضعیف ترین قسمت خانه باتری می گردد که معمولاً الکترولیت از آنجا خارج می شود و نشانه آن بوجود آمدن سفیدک های کوچکی (سولفاته) در اطراف پوسته باتری می شود.
۲- جلوگیری از خروج الکترولیت مایع از درب
اگر سوراخ روی درب باتری یک سوراخ ساده باشد ممکن است در اثر شتاب دهی ناگهانی یا ترمز شدید، مایع الکترولیت از طریق این سوراخ ها خارج شده و میزان سطح الکترولیت در باتری پایین بیاید.
بنابراین درب خانه باتری را طوری طراحی می کنند که علاوه بر اینکه قابلیت خروج بخارهای داخل باتری را داشته باشد، از خارج شدن الکترولیت مایع جلوگیری کند.
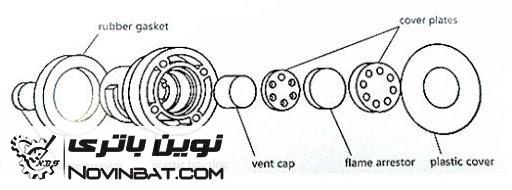
دو نوع از طرح های بکار رفته برای درب خانه باتری در شکل های زیر آمده است:
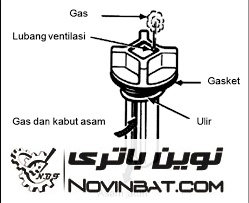
همانطور که ملاحظه می گردد مجاری مارپیچی برای سوراخ درب خانه باتری در نظر گرفته شده است که با توجه به قابلیت بخار، می تواند از این مجاری عبور کرده و از آن خارج شود اما مایع الکترولیت پس از برخورد با قسمت بالایی مارپیچ به سمت پایین بر می گردد.
البته برخی باتری های موجود در ایران فقط با قرار دادن یک مانع ساده زیر سوراخ درب خانه باتری، این کار را انجام می دهند که مسلماً کارایی آن به اندازه طرح هایی که در اشکال فوق ملاحظه می گردد، نمی باشد.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
قطب های باتری (Terminal Post of Battery)
هر باتری دارای دو قطب اصلی و ثابت (برعکس کاتد و آند که با توجه به جهت شارژ تغییر می کنند و ثابت نیستند) می باشد.
باید توجه داشت که هر خانه باتری خود دارای دو قطب مجزا می باشد. در باتری های غیر قابل تعمیر (باتری های متداول امروز) این قطب ها زیر درپوش بالایی باتری قرار گرفته و دیده نمی شوند، یعنی یک باتری دوازده ولتی دارای دوازده قطب می باشد که شش قطب آن مثبت و شش قطب آن منفی است.
دو قطب از دوازده قطب باتری، قطب های اصلی هستند که خارج از قاب باتری قابل مشاهده است و سایرین در زیر درپوش قرار دارند. در مورد نحوه اتصال خانه های باتری در آینده صحبت خواهد شد. از این به بعد منظور از قطب، همان قطب های اصلی باتری خواهد بود. قطب های باتری محل خروج جریان برق از باتری در زمان مصرف شدن و محل ورود جریان برق به باتری در زمان شارژ شدن باتری می باشد.
با توجه به جهت جریان برق یک قطب را قطب مثبت و دیگری را قطب منفی می نامند که این یک مورد ثابت در مورد باتری ها است یعنی جای قطب های مثبت و منفی باتری عوض نمی شود.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
شناسایی قطب های مثبت و منفی
با توجه به اینکه در هنگام نصب باتری روی اتومبیل قطب منفی به بدنه و قطب مثبت به کابل استارت (اتومات استارت) متصل می گردد تشخیص دو قطب باتری از یکدیگر حائر اهمیت می باشد.
.
علامت های قطب مثبت: علامت + – POS – P – رنگ درپوش یا علامت، قرمز رنگ است – ضخامت بیشتر از قطب دیگر
علامت های قطب منفی: علامت – – NEG – N – رنگ درپوش یا علامت، سیاه یا آبی رنگ است – ضخامت کمتر از قطب دیگر
.
در صورتیکه هیچ یک از علامت های ذکر شده وجود نداشت (پاک شده بود و یا قابل تشخیص نبود) می توان با یک آزمایش ساده قطب ها را از یکدیگر تشخیص داد. یک سیم که دو سر آن لخت شده باشد تهیه کنید. یک سر سیم را به یکی از قطب های باتری متصل کنید و سر دیگر آن را در داخل الکترولیت یکی از خانه ها قرار دهید.
ملاحظه خواهید کرد که اطراف سیم حباب هایی به وجود می آید. این آزمایش را با قطب دیگر نیز انجام دهید. هر کدام از قطب هایی که حباب بیشتری در اطراف سیم داخل الکترولیت تولید کرد آن قطب، قطب منفی می باشد.
تذکر: این آزمایش فقط جهت موارد ضروری می باشد. تکرار آن باعث خراب شدن باتری می گردد.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
توجه: هیچگاه دو سیم از دو قطب را همزمان وارد یک خانه باتری نکنید چون ممکن است در اثر اتصال بین دو سیم (اتصال کوتاه) الکترولیت باتری (آب اسید) به صورت شما پاشیده شود.
الکترولیت باتری
الکترولیت باتری سربی-اسیدی محلول رقیق شده اسید سولفوریک می باشد. لازم است مقدار آب و اسید سولفوریک به دقت و نسبت معین با یکدیگر مخلوط شوند. این نسبت معین به صورت جدول زیر می باشد:
| واحد اندازه گیری | مقدار آب H2O | مقدار اسید سولفوریک H2SO4 |
| پیمانه ای | ۸ پیمانه | ۳ پیمانه |
| درصد حجمی | %۷۳ | %۲۷ |
| درصد وزنی | %۶۳ | %۳۷ |
توجه: در اکثر باتری سازی ها (مراکز برق و باتری خودرو) نسبت آب در محلول را سه به چهار انتخاب می کنند. یعنی به ازای هر یک پیمانه اسید سولفوریک، سه پیمانه آب اضافه می کنند که معادل ۷۵ درصد آب و ۲۵ درصد اسید می باشد که نزدیک به نسبت حجمی ۷۳ درصد به ۲۷ درصد است گرچه دقیق نیست.
چگالی (جرم حجمی) این محلول در دمای ۱۵ درجه سانتی گراد معادل ۱٫۲۸ گرم بر سانتی متر مکعب (یا همان ۱۲۸۰ کیلوگرم بر مترمکعب) می باشد. این عدد با تغییرات دما و فشار هوا تغییر می کند.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
تاثیر دما بر الکترولیت باتری خودرو
به ازای افزایش هر ۱٫۵ درجه دما مقدار ۰٫۰۰۱ گرم بر سانتی متر مکعب (یک کیلوگرم بر متر مکعب) از عدد اصلی ۱٫۲۸ گرم بر سانتی متر مکعب (۱۲۸۰ کیلوگرم بر متر مکعب) کم می شود. مثلاً جرم حجمی استاندارد در دمای ۲۱ درجه عبارتند از:
| ۶=۲۱-۱۵ | میزان اختلاف دمای محیط از دمای استاندارد |
| ۴=۱٫۵/۶ | افزایش چگالی به ازای ۶ درجه افزایش دما |
| ۱۲۷۶=۱۲۸۰-۴ | کاهش چگالی بخاطر افزایش دما |
یعنی در دمای ۲۱ درجه سانتی گراد جرم حجمی الکترولیت باید ۱۲۷۶ کیلوگرم بر متر مکعب (۱٫۲۷۶ گرم بر سانتی متر مکعب) باشد.
دانستن مقدار چگالی به ما کمک می کند که بفهمیم باتری به شارژ شدن نیاز دارد یا خیر.
مثال: چگالی الکترولیت در دمای ۲۷ درجه ۱۲۱۰ کیلوگرم بر متر مکعب می باشد. آیا این باتری به شارژ نیاز دارد یا خیر؟
| ۱۲=۲۷-۱۵ | میزان اختلاف دمای محیط از دمای استاندارد |
| ۸=۱٫۵/۱۲ | افزایش چگالی به ازای ۱۵ درجه افزایش دما |
| ۱۲۷۲=۱۲۸۰-۸ | چگالی یک الکترولیت استاندارد اگر دما را به ۲۷ درجه برسانیم |
| ۱۲۱۸=۱۲۱۰+۸ | چگالی همین الکترولیت اگر دما را به ۱۵ درجه برسانیم |
چون چگالی یک الکترولیت استاندارد اگر دما را به ۲۷ درجه برسانیم معادل ۱۲۷۲ می شود و چگالی الکترولیت ما در همین دما ۱۲۱۰ است پس باتری نیاز به شارژ دارد. به عبارت دیگر چون چگالی همین الکترولیت اگر دما را به ۱۵ درجه برسانیم معادل ۱۲۱۸ است و این عدد کمتر از چگالی استاندارد یعنی ۱۲۸۰ هست پس باتری دشارژ می باشد.
نکته: برای تشخیص شارژ بودن باتری معمولاً محدوده ای وجود دارد که طبق آن باید نظر داد.
توجه: هیچگاه از آب لوله کشی برای تهیه الکترولیت استفاده نکنید. آب مورد استفاده باید آب خالص (آب مقطر) باشد.
می توان این آب را از لوازم یدکی ها در بطری های آماده تهیه کرد یا از آب جوشیده و سپس خنک شده استفاده نمود یا اینکه برفک یخچال را آب کرده از آن استفاده کنیم.
نکته: هنگام تهیه الکترولیت ابتدا آب را در یک ظرف پلاستیکی (لگن) ریخته سپس به آرامی اسید را به آن اضافه کنید. حتی بهتر است یک سطح شیب دار پلاستیکی تهیه کرده و اسید را از بالا روی آن بریزید تا به آرامی وارد لگن آب شود. این کار بدلیل انجام واکنش شدید بین آب و اسید سولفوریک و گرمازا بودن این واکنش می باشد. در صورت اضافه شدن سریع اسید به آب، دمای محلول بشدت بالا رفته و به حد جوش می رسد و محلول به اطراف می پاشد.
نکته: سطح الکترولیت در هر خانه باتری باید در حد معین (بالاتر از خط MIN و پایین تر از خط MAX روی بدنه باتری) باشد.
اگر الکترولیت بیشتر از حد استاندارد باشد احتمال ریختن آن در شتاب های ناگهانی یا ترمز های شدید وجود دارد و اگر کمتر از حد استاندارد باشد قسمتی از صفحه باتری در معرض هوا قرار گرفته و به مرور خراب می شود. البته مراقبت و بازدید سطح الکترولیت، فقط در مورد باتری های اسیدشارژ الزام دارد و در مورد باتری جدید سیلد، کاربر نه دسترسی به الکترولیت باتری دارد و نه نیازی به بازدید و مراقبت از باتری است.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
ظرفیت باتری
روش های مختلفی برای تعیین مقدار ظرفیت یک باتری توسط انجمن بین المللی باتری (Battery Council International (BCI)) ارایه شده است که چهار روش زیر به ترتیب اهمیت عبارتند از:
***وب سایت رسمی انجمن بین المللی باتری (BCI): https://Batterycouncil.org/ ***
۱- آمپر گرداندن میل لنگ در شرایط سرد یا تست باتری در شرایط سرد (Cold Cranking Amps (CCA)):
این مقدار نشان دهنده توانایی یک باتری برای کار در شرایط سرد می باشد و برابر است به مقدار آمپری که یک باتری در دمای صفر درجه فارنهایت (۱۷٫۸- درجه سانتی گراد) می تواند از خود خارج کند بدون اینکه ولتاژ باتری کمتر از ۷٫۲ ولت شود.
۲- آمپر گرداندن میل لنگ یا تست باتری (Cranking Amps (CA)):
مانند روش قبل اما در دمای ۳۲ درجه فارنهایت (تقریباً ۷٫۷ درجه سانتی گراد) است. رابطه ای تقریبی وجود دارد که می توان عدد CCA را به CA تبدیل نمود که این رابطه عبارت است از: CA=CCA*1.25
۳- ظرفیت ذخیره باتری (Reserve Capacity=RC)
مدت زمانی که باتری بتواند در دمای ۸۰ درجه فارنهایت (۲۶٫۷ درجه سانتی گراد) جریان ۲۵ آمپر بدهد بدون اینکه ولتاژ کل آن کمتر از ۱۰٫۵ ولت شود. یک باتری سالم باید بتواند در صورت خراب شدن سیستم شارژ (دینام) در مدت زمان نسبتاً طولانی، نیاز های الکتریکی خودرو را مرتفع کند.
۴- آمپرساعت (Ampere hour):
حاصل ضرب شدت جریان در زمانی است که باتری می تواند این شدت جریان را تامین کند. واحد آن آمپرساعت (AH) می باشد.
ساعت * شدت جریان = ظرفیت
مثلاً اگر ظرفیت یک باتری ۶۰ آمپرساعت (۶۰ AH) است می تواند مدت زمان شصت ساعت جریان یک آمپری را تامین کند (۶۰ * ۱ = ۶۰) یا مدت یک ساعت جریان شصت آمپری را تامین کند (۱ * ۶۰ = ۶۰) یا مدت بیست ساعت جریان سه آمپری را تامین کند (۲۰ * ۳ = ۶۰).
نکته: هنگامی که آمپر (جریان) از باتری کشیده می شود (باتری زیر بار) نباید ولتاژ باتری کمتر از ۱۰٫۵ ولت شود (تست صحت عملکرد باتری)
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
عوامل موثر در تغییر مقدار ظرفیت باتری
۱- تعداد صفحات باتری
۲- مساحت صفحات باتری
۳- دما
۴- مقدار الکترولیت
۵- چگالی الکترولیت
پلاک باتری
برای استفاده بهتر از هر وسیله ای لازم است اطلاعاتی در مورد آن وسیله به ما داده شود. محلی که این اطلاعات در آنجا ثبت می شود را پلاک مشخصات می گویند. باتری ها نیز دارای پلاک مشخصات می باشند. شرکت های تولید کننده باتری، روش های مختلفی را برای تهیه و ارائه پلاک باتری دارند.
متداول ترین روش برای این مهم این است که تمام اطلاعات مورد نیاز را روی پوسته باتری درج (حک یا به صورت برچسب) می کنند.
در اینجا سعی برآن است که تمام اطلاعاتی که می توان به عنوان یک مشخصه باتری ثبت کرد، بیان کنیم:
۱- کد استاندارد باتری: هر نوع باتری تولید شده دارای یک کد استاندارد می باشد. متداول ترین نوع استاندارد برای باتری ها، استاندارد DIN (استاندارد آلمان) است.
۲- ولتاژ باتری: یکی از مهمترین مشخصه های یک باتری که حتماً تمام تولید کنندگان باتری، باید آن را روی باتری درج کنند، مقدار ولتاژ خروجی باتری می باشد.
ولتاژ باتری های مخصوص خودرو، بین ۶ ولت تا ۲۴ ولت می باشد. البته ولتاژ باتری های تولید شده برای خودروهای سبک و سنگین فقط ۱۲ ولت است و برای ولتاژ ۲۴ ولت (که مخصوص برخی از خودروهای سنگین می باشد) باید دو عدد باتری ۱۲ ولت را با هم سری کنیم.
۳- ظرفیت باتری: ذکر حداقل یکی از موارد یاد شده، که نشان دهنده ظرفیت باتری می باشد. در ایران معمولاً آمپرساعت (AH) و تست در شرایط سرد (CCA) ذکر می شود.
۴- سایز باتری: با توجه به اینکه هر خودرو (اعم از ایرانی و خارجی) دارای فضای محدود و خاص، جهت نصب باتری است، حتماً باید ابعاد باتری مشخص باشد. برای این امر می توان به کاتالوگ های کارخانه سازنده باتری مراجعه نمود.
۵- تاریخ تولید باتری: با توجه به محدود بودن عمر باتری لازم است مصرف کننده از تاریخ تولید و تاریخ مصرف باتری آگاه باشد. شرکت های تولید کننده روش های مختلفی برای ارائه این دو تاریخ دارند.
۶- شماره سریال باتری: سریال حک شده روی بدنه باتری است. تولید کنندگان باتری، برای هر باتری، یک سریال مخصوص به خود قرار می دهند. این سریال جهت خدمات پس فروش (گارانتی) بسیار حائز اهمیت است.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
نشان دهنده میزان الکترولیت و چگالی (جرم حجمی) در باتری
همانطور که ذکر شد ارتفاع سطح الکترولیت باید در حد معینی باشد. برای تشخیص این مطلب روی بدنه سفید رنگ باتری ها (باتری هایی که سطح الکترولیت از بیرون آن مشخص است) دو خط قرار داده شده است که یکی بیشترین حد (MAX) و دیگری کمترین حد (MIN) را مشخص می کند. میزان الکترولیت حتماً باید بین این دو خط باشد.
در باتری هایی که دارای بدنه سفید رنگ نیستند یا اینکه سطح الکترولیت از بیرون مشخص نیست تشخیص این امر کمی مشکل است. بنابراین در بعضی از این نوع باتری ها، نشان دهنده ای را روی خانه باتری قرار داده اند، که می توان با مشاهده آن، سطح آب باتری را تشخیص داد. در برخی دیگر از این نوع باتری ها، نشان دهنده جرم حجمی الکترولیت (هیدرومتر) نصب شده است.
در این نوع باتری ها، کاربر به راحتی با مشاهده این نشان دهنده به شارژ بودن و یا دشارژ بودن باتری (بدلیل تغییر رنگ نشانگر) پی می برد.
استارت خودرو
وظیفه استارت، راه اندازی و چرخش موتور برای روشن کردن خودرو می باشد.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
اساس کار استارت خودرو
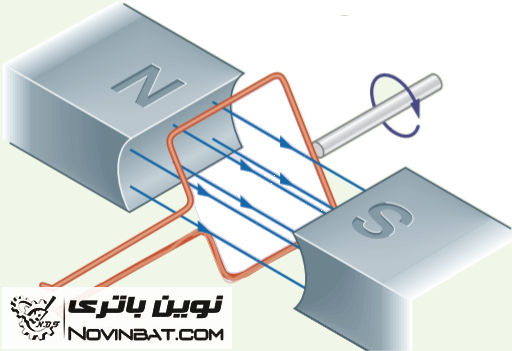
همانطور که می دانیم هر سیم حامل جریان برق، در اطراف خود میدان مغناطیسی تولید می کند. اگر در یک میدان مغناطیسی یک میله هادی حامل جریان برق قرار دهیم، میدان مغناطیسی میله هادی با میدان مغناطیسی اصلی بر هم نیرو وارد کرده در نتیجه باعث حرکت میله هادی می شود.
اگر بجای یک میله هادی از یک قاب (N و S ثابت) و دو نیم حلقه (نقش میله هادی) مطابق شکل استفاده کنیم هنگامی که جریان از طریق دو نیم حلقه به قاب ارسال شود (با توجه به جهت جریان در داخل قاب میدان مغناطیسی بوجود آمده) اگر تشکیل قطب های همنام دهد باعث دفع قاب و اگر تشکیل قطب های غیر همنام دهد باعث جذب قاب می شود. در موتورهای الکتریکی جهت جریان را طوری انتخاب کرده که تشکیل قطب های همنام دهد و باعث چرخش قاب شود.
.
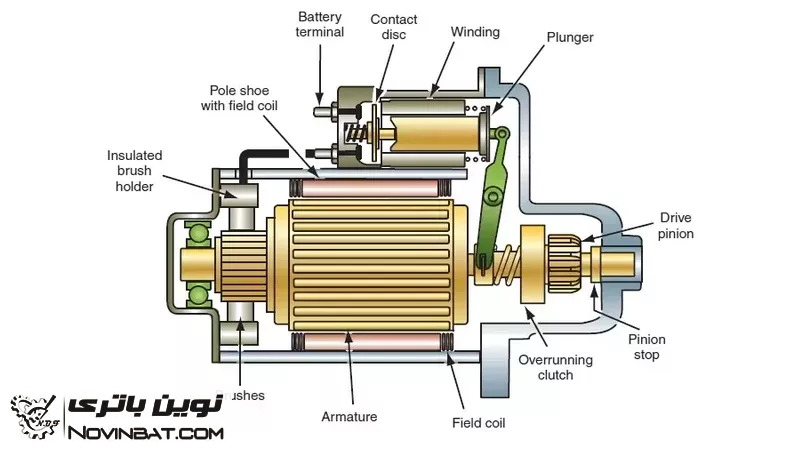
اجزای استارت خودرو
.
۱- بالشتک های استارت: وظیفه آنها تولید میدان مغناطیسی بسیار قوی است. با توجه به نوع کلاف های بالشتک ها، جریان زیادی از آن عبور کرده و باعث تولید میدان مغناطیسی می شود. استارت ها با توجه به نوع اتصال بالشتک ها، به دو نوع سری و موازی طراحی می شوند.
- نوع سری: در این نوع از بالشتک ها جریان برق وارد کلاف های بالشتک شده و پس از عبور از بالشتک ها از طریق زغال مثبت وارد کلاف های آرمیچر شده و از طریق زغال منفی به بدنه استارت متصل شده و مدار استارت کامل می شود.
- نوع موازی: در این استارت جریان برق باتری ابتدا وارد زغال های مثبت شده و از طریق زغال مثبت به دو بالشتک مجاور هم رسیده و از طریق بالشتک متصل بدنه می شود یعنی بالشتک ها نسبت به آرمیچر موازی می باشند.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
۲- آرمیچر استارت: با عبور جریان زیاد از آرمیچر، میدان مغناطیسی قوی ایجاد می شود و طبق قانون موتورهای الکتریکی میدان تولیدی آرمیچر با میدان تولیدی بالشتک ها بر هم نیرو وارد می کنند و باعث چرخش آرمیچر می شوند.
۳- زغال های استارت: جریان عبوری بالشتک ها و آرمیچر از طریق زغال انجام می گیرد. جنس زغال ها از مس و کربن بوده و مقدار مس آن بیشتر است تا هم اتلاف انرژی کمتر شود هم در برابر عبور جریان زیاد و گرما مقاومت داشته باشد. استارت ها در دو نوع دو زغاله و چهار زغاله تولید می شوند.

۴- دنده استارت: دنده استارت همانند دنده واسطه عمل کرده و وظیفه انتقال نیروی استارت به فلایویل را دارد. استارت دارای یک مجموعه به نام کلاچ یک طرفه می باشد که نیرو را در یک جهت منتقل کرده و در جهت دیگر به صورت هرز می گردد.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
انواع استارت
۱- استارت دنده مارپیچی: در این نوع استارت اتومات، جدا از استارت است. عیب این نوع استارت ها این بود که گاهی دنده استارت پس از روشن شدن موتور درگیر باقی می ماند. هنگامی که برق سوییچ، اتومات را تحریک می کند از طریق اتومات استارت در همان لحظه جریان کمی به موتور استارت رسیده و استارت به آرامی می چرخاند.
در این حالت دنده استارت روی شَفت، حرکت مخالف کرده و به دنده فلایویل نزدیک می شود.
در این لحظه جریان اصلی برق، از طریق کنتاکت اتصال دهنده، به موتور استارت رسیده و باعث می شود نیرویی به دنده استارت وارد گردد که همان نیروی گریز از مرکز است که مخالف جریان شفت آرمیچر بوده و باعث درگیری کامل و از بیرون نزدن دنده استارت می شود و درنتیجه سبب چرخش فلایویل می شود. هنگامی که موتور روشن شد، دور دنده فلایویل، دنده استارت را به عقب می راند.
در پشت دنده استارت یک فنر بزرگ پیچشی تعبیه شده و ضربه دنده استارت را مستهلک می کند.
۲- استارت مارپیچی کشویی: در این استارت اتومات استارت دو وظیفه در حین راه اندازی موتور استارت دارد:
- ارسال برق اصلی باتری به موتور استارت
- به حرکت در آوردن (به جلو بردن) دنده استارت جهت درگیری با دنده فلایویل برای گردش موتور
عملکرد اتومات استارت در نوع استارت مارپیچی بدین شکل است که اتومات استارت دارای دو عدد سیم پیچ بوده که یکی از سیم پیچ ها نازک با تعداد دور زیاد و به صورت موازی وصل شده (سیم پیج نگهدارنده) و دیگری از سیم ضخیم با تعداد دور کم و بصورت سری متصل شده است (سیم پیچ کِشنده).
هنگامیکه سوئیچ را در مرحله استارت قرار می دهیم جریان از طریق سوییچ به سلونوئید استارت رسیده که به سر مشترک سیم پیچ نگهدارنده و کشنده وصل شده است. در ابتدا جریان از هر دو سیم پیچ عبور کرده و باعث تولید میدان مغناطیسی قوی شده که این حالت باعث جذب پیستون یا پلانچر اتومات به طرف داخل می شود و با حرکت پیستون دو عمل صورت می گیرد:
- اتصال دیسک کنتاکت دهنده به پیچ های M و B که B اتومات به برق باتری و M اتومات به موتور استارت وصل شده. برق باتری از طریق اتومات وارد موتور استارت شده و در این حالت سیم پیچ کشنده چون به صورت سری بوده از مدار خارج می شود و سیم پیچ نگهدارنده، پیستون را نگه می دارد و باعث چرخش استارت می شود.
- از طرف دیگر حرکت پیستون یا پلانچر به طرف داخل باعث حرکت ماهک دنده استارت به طرف جلو شده و دنده استارت با دنده فلایویل درگیر می شود. با قطع برق سوییچ از حالت استارت، برق اتومات استارت قطع شده و میدان مغناطیسی آن از بین می رود و همین امر باعث می شود فنر برگشت دهنده، پیستون را به جلو برده و دنده استارت (با توجه به مکانیزم خود) به عقب برگردد. اتصال کنتاکت دهنده نیز ترمینال B و M را از هم جدا می کند و استارت از چرخش می ایستد. عاملی که وجود اتومات استارت را یک ضرورت برای استارت می کند این است که عبور جریان خیلی زیاد باعث می شود، هیچ کلید و سوییچی توان تحمل این جریان زیاد را نداشته باشند و در اثر ایجاد حرارت بالا، ذوب شوند.
۳- استارت آرمیچر کشویی: این نوع استارت ها برای کامیون ها و اتوبوس ها استفاده می شوند که دارای سیم پیچ کشنده و سیم پیچ کمک می باشند و مجموعه آرمیچر جهت درگیر شدن با فلایویل حرکت می کنند. همچنین دارای کلاچ چند صفحه ای هستند که در زمان استارت زدن، حرکت را انتقال دهند و در زمان روشن شدن حرکت را منتقل نکنند.
۴- استارت گیربکسی: استارت های جدید و متداول امروز برای خودروهای سبک (سواری) می باشد. دارای استهلاک پایین و کارایی بالاتری نسبت به دیگر مدل ها بوده و به نیروی کمتری جهت روشن کردن خودرو نیازمند است.
برای بدست آوردن گشتاور بیشتر جهت چرخاندن راحت تر موتورهایی که تعداد سیلندر بیشتر دارند و یا حجم موتور آنها بالا است از چرخ دنده سیاره ای استفاده می کنند. قطعه ای بنام گیربکس به واحد استارت اضافه گذشته که دور آرمیچر استارت، توسط این واحد چرخ دنده ها، به گشتاور تبدیل گشته و بنابراین حجم و فضای اشغالی توسط استارت در اتومبیل کاهش و از طرفی جریان مصرفی نیز کم می شود.
دینام های آلترناتور
دلایل ظهور دینام های آلترناتور
یکی از معایت دینام های جریان مستقیم این است که این دینام ها در دورهای پایین موتور، قادر به شارژ باتری نمی باشند.
امروزه مصرف کننده های برقی در خودروها زیاد شده است و از طرفی ترافیک شهر ها باعث می شود که موتور یک اتومبیل مدت ها درجا کار کند و در این حالت دور دینام پایین است که باعث می شود دینام های جریان مستقیم نتوانند جوابگوی شارژ باتری باشند، به همین دلیل امروزه دینام های جریان مستقیم از رده خارج شده و از دینام های آلترناتور استفاده می شود.
اساس کار دینام های آلترناتور مانند دینام های جریان مستقیم است. در دینام های آلترناتور نیز بر اثر قطع قوای مغناطیسی جریان القایی بوجود می آید ولی با این تفاوت که در دینام های جریان مستقیم آهن رباها به بدنه دینام پیچ و ثابت شده بود و سیم پیچ های تولید جریان، داخل حوزه مغناطیسی حرکت می کردند ولی در دینام های آلترناتور آهن ربا دوار است و سیم پیچ های تولید جریان ثابت می باشند.
آهن ربای دوار را روتور و سیم پیچ ثابت را استاتور می نامند.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
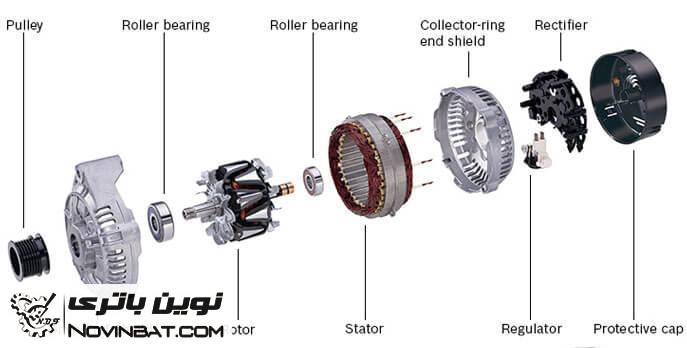
قطعات دینام
۱- روتور: روتور مجموعه ای است که وظیفه تولید حوزه مغناطیسی را در آلترناتور به عهده دارد. روتور از یک محور تشکیل شده که جلوی آن دارای رزوه برای بستن مهره نگهدارنده پولی است. در قسمت وسط روتور یک سیم پیچ روی محور، به صورت پرس قرار گرفته است. این سیم پیچ روی یک حلقه پلاستیکی پیچیده شده تا از اتصال آن با بدنه جلوگیری شود.
روی این سیم پیچ چنگک های فلزی از دو طرف قرار می گیرد. این چنگک ها نیز روی محور قرار گرفته اند. دو سر سیم پیچ به دو حلقه مسی که در انتهای محور قرار دارد وصل می شوند (کلکتورها). انتهای محور و پشت کلکتورها یک بلبرینگ به صورت پرسی سوار شده که این بلبرینگ درون محل خود داخل پوسته عقب قرار می گیرد. اگر به سر سیم پیچ روتور، جریان برق متصل کنیم چنگک ها آهن ربا می شوند چون لبه این چنگک ها بر عکس یکدیگر نسبت به سیم پیچ قرار گرفته اند.
در نتیجه هر دو لبه کناری در میان قطب های S و N می شوند و بین آنها میدان مغناطیسی ایجاد می شود. در قسمت جلوی محور یک پولی توسط خار با آن درگیر می شود. دور این پولی تسمه قرار می گیرد که نیروی میل لنگ توسط این تسمه به محور دینام منتقل شده و باعث گردش آن می شود.
۲- استاتور: استاتور مجموعه سیم پیچی می باشد که در اثر برخورد حوزه مغناطیسی با آن جریان الکتریسیته بوجود می آید.
این سیم پیچ ها باید دور روتور قرار گیرند تا داخل حوزه مغناطیسی باشند و با چرخش حوزه دوار، الکترون ها در این سیم پیچ ها حرکت کنند. استاتور دارای یک بدنه فلزی می باشد که داخل این بدنه فلزی شیار هایی وجود دارد. سیم پیچ ها داخل این شیار ها پیچیده می شوند.
چون در اثر کار کردن و گرمای حاصل از موتور، بدنه استاتور داغ می شود، بدنه استاتور را از ورق های نازک که به یکدیگر پرس شده اند، می سازند. داخل شیار های استاتور ورقه های عایق قرار گرفته است تا از اتصال سیم پیچ با بدنه استاتور جلوگیری شود. اگر یک سیم پیچ را داخل شیار های استاتور بپیچیم و دو سر آن را خارج کنیم فقط یک سر جریان تولید می کند.
به این استاتور اصطلاحاً استاتور تک فاز می گویند. در بعضی از دینام ها برای تولید جریان بالاتر از سه سیم استفاده می کنند. در این حالت سه سیم در زاویه معینی نسبت به یکدیگر در بدنه استاتور پیچیده می شوند. اصطلاحاً به این نوع استاتور سه فاز گفته می شود. در استاتور سه فاز سه سر خروجی خواهیم داشت که در نتیجه بازدهی بالا می رود.


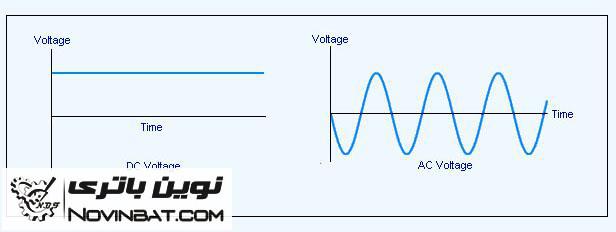
۳- دیود: آلترناتور، مولد جریان متناوب می باشد. جریان متناوب به جریانی گفته می شود که مسیر حرکت الکتورن ها در هادی دائماً تغییر می کند. اگر چنین حالتی باشد دیگر قطب منفی و مثبت در این هادی مفهومی نخواهد داشت لذا بوسیله این جریان نمی توان باتری را شارژ کرد زیرا الکترون هایی که به سوی باتری سرازیر می شوند با عوض شدن مسیر جریان دوباره از آن خارج می گردند.
بنابراین باتری همیشه با جریان مستقیم شارژ می شود، یعنی جریانی که الکترون ها از یک سمت حرکت داشته باشند. چون جریان خروجی آلترناتور متناوب است با این جریان نمی توان باتری را شارژ کرد به همین خاطر در سر راه خروجی آلترناتور از دیود (یک سو کننده) استفاده می کنند. دیود قطعه ای الکترونیکی است که فقط جریان را از یک سمت از خود عبور می دهد و به این ترتیب جریان متناوب را به مستقیم تبدیل می کند.
نکته: جریان متناوب (AC) و جریان مستقیم (DC) دو نوعِ متفاوت از عبور جریان الکتریسیته یا شار الکتریکی در مدار هستند. در جریان مستقیم، بار الکتریکی در یک جهت عبور میکند. در جریان متناوب، بار الکتریکی به طور تناوبی جهت عوض میکند. ولتاژ نیز در مدارهای AC گاهی اوقات برعکس میشود زیرا که جریان، جهت عوض میکند. AC چند خاصیت مفید دیگر نیز دارد، از جمله تغییر سطح ولتاژ توسط تنها یک قطعه مبدل گونه (ترانسفورماتور)، چیزی که باعث میشود ابزار AC اولین انتخاب ما برای انتقال برق به فاصله های دور باشد.
.
جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه
.
۴- پوسته: آلترناتور از دو پوسته جدا از هم تشکیل شده است که معمولاً از جنس آلومینیوم می باشند. بدنه فلزی استاتور، ما بین این دو پوسته قرار می گیرد و توسط چند پیچ بلند دو پوسته روی یکدیگر محکم می گردند. دو عدد بلبرینگ برای گردش محور روتور درون این دو پوسته قرار دارد.
یک بلبرینگ در پوسته جلویی و یک بلبرینگ روی محور روتور که در پوسته عقب آن قرار می گیرد.
۵- پولی و پنکه: مانند دینام های جریان مستقیم، قسمتی از محور روتور از پوسته جلویی آلترناتور بیرون است.
روی این قسمت یک پولی و پنکه قرار دارد که هر دو آنها توسط یک خار به محور روتور متصل می شوند.
جلوی آنها یک مهره بسته می شود و تسمه روی این پولی قرار گرفته که با گردش تسمه، پولی گردش کرده و باعث حرکت روتور می شود. همراه پولی، پنکه هم گردش کرده و هوا را از جلو وارد آلترناتور و از عقب آن خارج می کند تا باعث خنک شدن قطعات آلترناتور گردد. در بعضی از آلترناتورها پنکه در قسمت داخل آلترناتور و پشت روتور قرار دارد.
۶- زغال: در دینام های جریان مستقیم برق خروجی دینام ها از زغال ها عبور می کرد و چون این جریان زیاد بود، معمولاً زغالِ دینام جریان مستقیم، بزرگ بود ولی در آلترناتور جریان زیادی از زغال ها نمی گذرد و به همین خاطر زغال ها زیاد بزرگ نیستند (کوچک تر از زغال استارت). این زغال ها در یک جازغالی پلاستیکی قرار دارند و سرِ زغال ها روی کلکتور انتهای روتور، قرار می گیرند.
پشت این زغال ها یک فنر کوچک وجود دارد که همیشه زغال ها را بر روی کلکتور می فشارد. در بعضی از آلترناتورها که آفتامات آنها ترانزیستوری (دینام های جدید و متداول امروز) می باشد مجموعه آفتامات و جازغالی و زغال روی یکدیگر نصب می شوند.
پایان
گردآورنده اولیه: احمد احمدی
بازنگری ، اصلاح ، ویرایش و به روز رسانی : ناصر فخار نوغانی
آخرین به روز رسانی جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه : اسفندماه ۱۳۹۸
آدرس اتحادیه صنف باتری سازان مشهد و حومه: مشهد – خیابان فدائیان اسلام – خیابان یاران – نبش یاران ۲۶
تلفن اتحادیه صنف باتری سازان مشهد و حومه: ۰۵۱۳۳۴۳۰۶۱۱
آدرس نوین باتری: مشهد – چهارراه خیام – خیابان شهید دستغیب ۲۸ – خیابان فرهاد ۲۷
تلفن نوین باتری: ۰۵۱۳۷۶۴۹۲۹۶ – ۰۵۱۳۷۶۴۹۶۰۹ – ۰۹۱۵۳۸۲۸۵۰۸
وب سایت: Novinbat.com


























با تشکر من مححق در خصوص نیروگاه های خورشیدی هستم. دنبال مشخصه جریان-ولتاژ(V-I )کلی یک باطری بودم که در جزوه شما موچود نبود. اما در خصوص باطری ودینام ماشین مطالب خوبی ارائه دادین و برای آشنایی ابتدایی با این مطالب بسیار مفید است. با تشکر فراوان از زحمات شما اگر برایتان مقدور بود مشخصه جریان-ولتاژ(V-I ) یک باطری نمونه و عمومی را برایم بفرستید.
سلام جزوه به جا و خوبی هست ولی مطالب خیلی طولانی هست ای کاش جدا جدا هر مطلب رو میاوردین که هر کدوم جزوه اش مجازا بود.بهرحال ممنوتم ازتون
با عرض سلام
مطالعه این جزوه برای کسانی که می خواهند در مشهد و حومه نسبت به اخذ جواز کسب اقدام کنند الزامی است چراکه منبع امتحان اتحادیه همین جزوه می باشد. این جزوه تا حد امکان خلاصه شده و حذف کردن بیشتر مطالب امکان پذیر نیست.
با تشکر
سلام من تعمیرگاه دارم و جزوه آموزشی اتحادیه صنف باتری سازان مشهد و حومه خیلی بهم کمک کرد چون هم از مواد و اجزای باتری ک حتما مواد شیمی ساخته شدن در آن را توضیح داده و هم انواع از دینام ماشین تا انواع استارت رو توضیح داده.